天使综合征的诊断及检测
诊断/检测.
天使综合征的 临床诊断是指先证者符合临床诊断标准共识和/或分子遗传学检测结果表明母源遗传的UBE3A等位基因表达或功能缺陷。约80%的AS患者可通过15q11.2-q13染色体区域的亲本特异性DNA甲基化印记分析进行检测,包括缺失、单亲二体(UPD)或印迹缺陷(ID)三种分子缺陷。不足1%的个体是由于细胞遗传学可见的染色体重排(即易位或倒位)所致。约11%的个体经序列分析可检测到UBE3A基因的致病性变异。因此,分子遗传学检测(甲基化分析和UBE3A序列分析)能够确定大约90%患者的遗传变异。其余10%具有AS典型表型特征的个体由于其遗传机制尚未明确,因此不适用于上述诊断检测。
明确诊断
符合临床诊断标准共识和/或分子遗传学检测结果表明母源遗传的UBE3A等位基因表达或功能缺陷(参见表 1)的患者可通过以下机制之一明确天使综合征的诊断:
- 由于下列机制之一导致的15q11.2-q13区域甲基化异常
- 母源遗传的15q11.2-q13 位点(包括UBE3A基因)缺失
- 父源15号染色体存在单亲二倍体
- 母源染色体15q11.2-q13位点存在印记缺陷
- 母源UBE3A基因存在致病性变异(点位突变)。
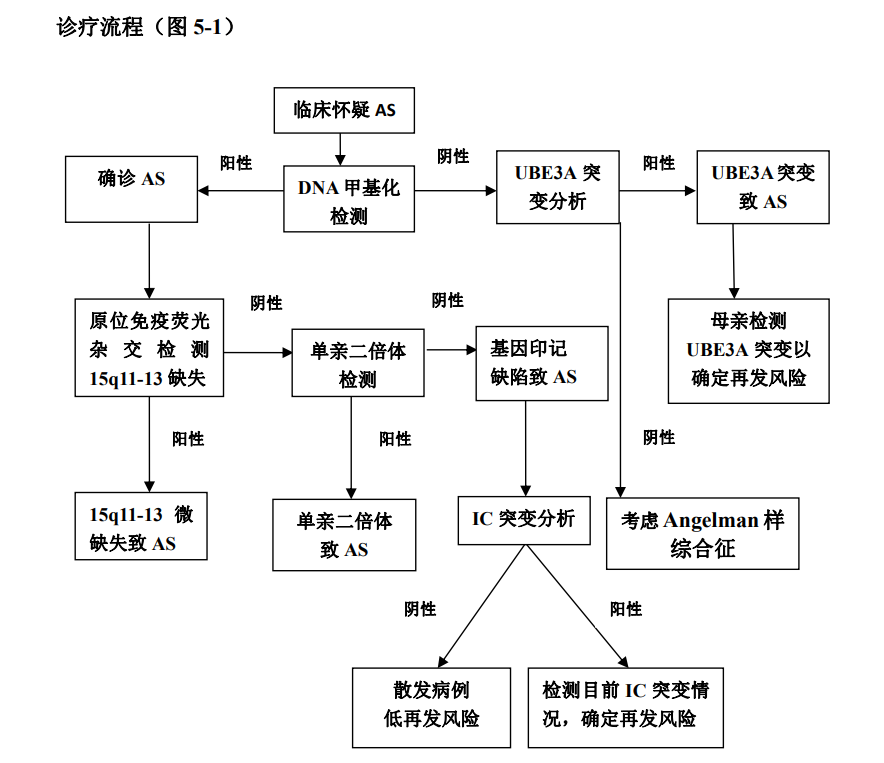
基于提示天使综合征的临床表现和实验室结果进一步进行分子遗传学检测,以明确诊断。
有临床症状但尚未进行过任何分子遗传学检测的个体:
- DNA 甲基化分析通常是首先选择的检测。由15q11.2-q13区域5-7Mb缺失,单亲倍二体(UPD)或印记缺陷(ID)引起的天使综合征个体仅具有未甲基化(即“父源”)条带(即亲本特异性DNA甲基化印记异常)。 DNA甲基化分析可明确约80%的天使综合征患者。备注:大多数商业化的DNA甲基化分析检测不能区分缺失、双倍体或ID导致的天使综合征。 需要进一步的检测来明确其分子机制(参见遗传咨询)。
- 如果DNA甲基化分析正常,可进行UBE3A基因检测或进行多基因Panel检测:
- UBE3A基因检测:首先开展序列分析。 如果并未鉴定到致病性变异,则可考虑进行靶向基因的缺失/重复分析。
- 多基因Panel检测:包含UBE3A和其他感兴趣基因(见鉴别诊断)分析具有天使综合征特征和正常DNA甲基化分析结果的个体。 备注:包括的基因以及多基因检测包的敏感性会随实验室和检测时间的不同而存在差异。
- . 对于具有天使综合征特征的个体而言,如果UBE3A检测(和/或使用 Panel检测)未能明确诊断,则可以考虑包括全外显子组测序,全基因组测序和线粒体测序在内的更全面的基因组检测(如果可用)。有关全面的基因组检测的介绍,请点击此处。
通过染色体芯片(CMA),荧光原位杂交(FISH)或核型分析*发现的15q11.2-q13缺失个体,进行DNA甲基化分析,以确定缺失是否发生在母源15号染色体。
* 低于1%的天使综合征患者在细胞遗传学分析可见一条涉及15q11.2-q13区段的15号 染色体重排(即易位或倒位)。
表1.
天使综合征的检测方法
| 检测方法 | 15q11.2-q13缺失 | 单亲双倍体 | ID | UBE3A序列 | UBE3A缺失/重复 | 检测方法所发现的天使综合征患者比例2 |
| DNA 甲基化分析 3, 4 | X | X | X 5 | ~80% | ||
| MS-MLPA 6 | X | X | X | ~80% | ||
| FISH 7 | X | ~68% | ||||
| CMA 8 | X | X 9 | ~68% | |||
| UPD研究 10 | X | ~7% | ||||
| AS IC 缺失分析 11, 12 | X | ~3% | ||||
| UBE3A序列分析 | X 13 | ~11% 14 | ||||
| UBE3A基因的缺失/重复分析 11, 15 | X | 罕见 |
IC = 印记中心,ID = 印记缺陷,UPD = 单亲二体性
- 2. 11%的临床拟诊的天使综合征个体,在本表所述的所有检测结果都正常。
- 3.由15q11.2-q13区域5-7Mb缺失,单亲二体性(UPD)或印记缺陷(ID)引起的天使综合征个体仅具有未甲基化(即“父源”)条带(即亲本特异性的DNA甲基化印记异常)。
- 4. 不能区分遗传机制
- 5. 80%-90%IDs被认为是母体卵子发生或早期胚胎发生期间出现了表观遗传致病变异[Buiting 2010]。主要通过科研实验室可将ID分为IC缺失或表观遗传缺陷。
- 6. 甲基化特异性多重连接依赖性探针扩增(MLPA)可以与甲基化分析扩增法一同用于检测缺失 [Nygren et al 2005, Procter et al 2006, Ramsden et al 2010]。
- 7. 用D15S10和/或SNRPN探针进行的FISH分析方法可鉴定常见的15q11.2-q13缺失,但通常这种缺失不能被常规的细胞遗传分析方法检测到。
- 8. 染色体微阵列(CMA)的检测率略高于FISH,并可以提供有关缺失大小的详细信息。此外,它还提供了基因组其他部分的缺失和重复的信息。
- 9. 基于SNP的染色体芯片可以诊断全染色体和节段性/部分单亲二体,但不能检测所有单亲二体的情况。
- 10. 利用DNA多态性标记可检测UPD,这需要来自受累个体及其父母的DNA样品。
- 11. 基因靶向的缺失/重复分析可以检测基因内或其他靶向区域的缺失或重复。可以使用的方法包括:定量PCR、长片段PCR、多重连接依赖探针扩增技术(MLPA)和用于检测单个外显子缺失或重复的靶向基因微阵列技术。
- 12. AS印记中心(IC)的缺失分析可检测小缺失(6-200kb),占所有印记缺陷(IDs)病例的8%-15%[Buiting 2010]。
- 13. 序列分析可以检测出良性、可能良性、意义不确定、可能致病或致病性变异。致病性变异可包括基因内小缺失/插入和错义、无义和剪接位点变异;通常,不能检测外显子或全基因缺失/重复。有关序列分析结果解释中需要考虑的问题,请点击此处。
- 14. Malzac et al [1998], Fang et al [1999], Lossie et al [2001]
- 15. 尽管CMA通常检测15q11.2-q13的大片段缺失,但在极少数情况下,CMA可以检测到UBE3A基因多个外显子或整个基因缺失[Lawson-Yuen et al 2006, Sato et al 2007]。
11%或更多经临床诊断但未能检测出遗传异常的天使综合征患者,可能解释如下:
- 临床诊断错误
- 不在检测范围的UBE3A基因调控区致病性变异
- 影响UBE3A功能的其他未知机制或基因